У 2025 році Нобелівську премію з медицини отримали Мері Е. Брунков, Фред Рамсделл і Шимон Сакагучі за новаторські відкриття в галузі периферичної імунної толерантності — здатності імунної системи вибірково та специфічно не реагувати на білки (антигени) власного організму.
Це відкриття пояснює, як організм уникає самознищення й чому виникають аутоімунні хвороби.
Як зрозуміти, за що саме дали премію? І чи вплинуло це відкриття вже на медичну практику?Пояснює це патофізіолог, кандидат медичних наук і старший науковий співробітник Національної академії наук України – Василь Нагібін.
Як імунітет вчиться не атакувати себе
Наша імунна система не тільки бореться з інфекціями. У неї є важливі механізми стримування власної агресії. Так, ви все правильно прочитали. Якщо не буде балансу в організмі, то він знищить себе сам. Наша імунна система повинна знищувати власні інфіковані клітини та клітини, що зазнали мутацій, але не повинна атакувати здорові.
Баланс порушується? Немає так званої аутотолерантності, яка береже організм від самоушкоджень? Тоді виникають аутоімунні захворювання, адже імунна система починає знищувати власні здорові клітини. Наприклад, аутоімунними є цукровий діабет 1-го типу, розсіяний склероз, псоріаз тощо.
Як організм знає, що своє, що чуже? Завдяки центральній толерантності. Наш організм настільки розумний, що коли якийсь наш Т-лімфоцит — ключова клітина імунної відповіді — має потенціал атакувати власні тканини, він знищується ще до того, як потрапить у кровообіг.

Фото: EPA/UPG / Оголошення лауреатів Нобелівської премії з фізіології та медицини 2025 року: (зліва направо) Мері Е. Брунков, Фред Рамсделл і Шимон Сакагучі — за їхні відкриття на тему периферична імунна толерантність в Каролінському інституті в Сольні, Швеція, 6 жовтня 2025 р.
Що зробили нобелівські лауреати 2025 року
Троє вчених: Мері Е. Брунков, Фред Рамсделл і Шимон Сакагучі — довели, що існує окремий тип клітин, які не атакують, а стримують імунну відповідь.
Це Т-регуляторні клітини (Treg). Вони, як і інші Т-лімфоцити, формуються в тимусі, загрудинній залозі. Діють ці клітини в усьому організмі, підтримуючи так звану периферійну імунну толерантність.
«Раніше вважали, що головний механізм, який запобігає аутоімунним хворобам, — це центральна толерантність. Але ці дослідження показали, що її недостатньо. Імунна система має ще й активний механізм стримування, який працює вже після виходу клітин з тимуса», — пояснює Василь Нагібін.
Як це пояснити простіше? Глянути на ключовий експеримент, який провів японський учений Шимон Сакагучі. Він видаляв тимус у мишей. У результаті тварини хворіли на важкі аутоімунні порушення шкіри, нервової системи, імунітет мишей атакував їхні ж ендокринні органи.
Але! Коли цим мишкам переливали окрему групу Т-клітин з маркерами CD4 і CD25 — симптоми зникали. Так виявили новий тип клітин, що пригнічують надмірну імунну активність. Простіше кажучи, заспокоюють армію, яка готова махати шашками наліво й направо. Це стало ключовим доказом існування механізму периферійної толерантності.
Паралельно два інші дослідники, Мері Е. Брунков і Фред Рамсделл, теж працювали з мишами. Але з тими, що мали спадкові аутоімунні захворювання — так званими scurfy-мишами. Ті, як виявили дослідники, мали мутацію в гені FOXP3, що призводила до тяжких аутоімунних хвороб. Саме цей ген виявився критичним для формування Т-регуляторних клітин.
FOXP3 — це білок, що вмикає гени, потрібні для перетворення Т-лімфоцита на Treg. Якщо FOXP3 не працює — клітина не стає супресорною, тобто вона не пригнічує войовничі імунні клітини й імунна система втрачає самоконтроль.
«Вони не просто описали мутацію, — пояснює Нагібін, — а показали, що без FOXP3 клітина не може виконувати регуляторну функцію. Це дозволило визначати, візуалізувати та виділяти ці клітини з тканин».
Як працюють ці Т-регуляторні клітини
Василь Нагібін пояснює, що після формування в тимусі Treg-клітини діють на периферії — у тканинах, де можуть виникати імунні реакції. Якщо якась «помилкова» Т-клітина все ж пройшла контроль у тимусі, Treg може заспокоїти її реакцію вже поза його межами. Їхні функції:
- Treg приєднується до клітини і закриває її антигени, не даючи іншим лімфоцитам атакувати;
- Treg виділяє речовини, які пригнічують агресивні імунні клітини;
- Treg забирає з навколишнього середовища речовини, які необхідні іншим лімфоцитам для активації.
Уже зараз проводять сотні клінічних випробувань, які досліджують терапії на основі Treg — зокрема, для лікування цукрового діабету 1-го типу, розсіяного склерозу, псоріазу й онкохвороб.
«Це відкриття не дало миттєвих практичних результатів, — каже Нагібін, — але заклало основи для переосмислення того, як ми можемо керувати імунною системою і в разі її гіперактивності, і коли вона пасивна».
1. Онкологія: Т-регулятори як щит для пухлин
Пухлинні клітини часто вміють обманювати імунітет. Вони походять з власних тканин, отже, мають звичайні, свої білки на поверхні, поряд з мутованими. Т-регуляторні клітини розпізнають своє, тому гальмують атаку імунітету навіть проти ракових клітин.
«Цим активно користується пухлина: вона виробляє сигнали, які приваблюють Treg, створюючи навколо себе імунопривілейоване середовище, своєрідну зону захисту. Саме тому в імуноонкології зараз досліджують, як видалити або деактивувати Т-регулятори в самій пухлині. Зокрема, під час біопсії тканин лікарі іноді оцінюють рівень FOXP3 (маркера Treg), щоб передбачити ефективність імунотерапії», — додає Нагібін.
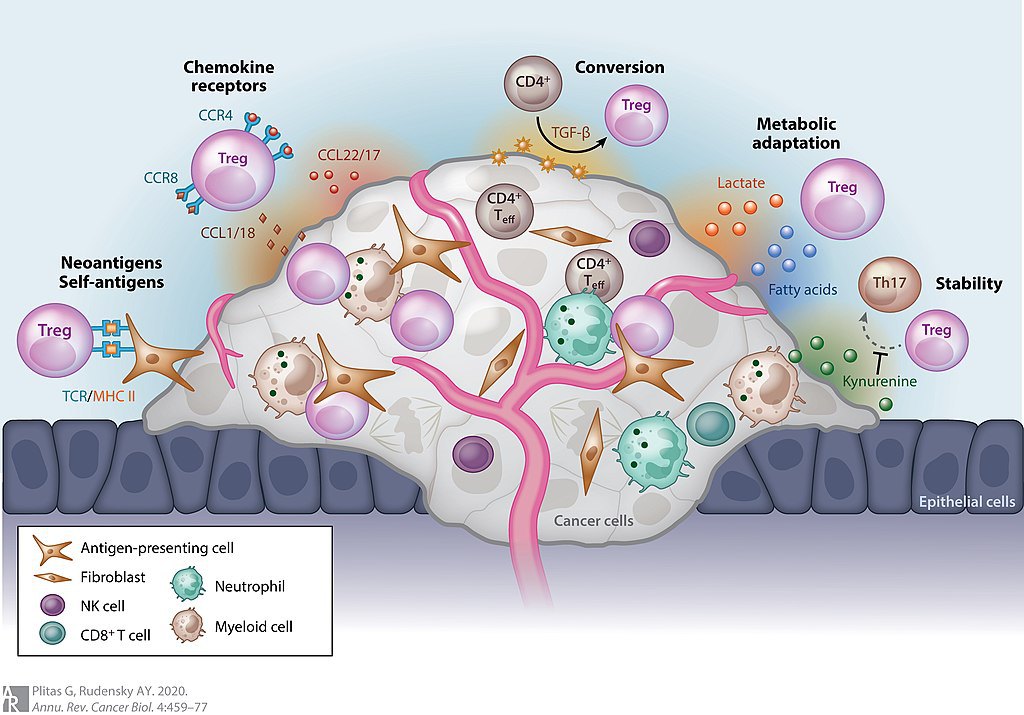
Фото: Вікіпедія /Doktorinternet / Симптом метелика на шкірі в пізній стадії системного червоного вовчака — типової аутоімунної хвороби.
Також ці клітини потенційно можуть допомогти запобігти імунному відторгненню трансплантованих органів. Це ще один важливий напрямок їхнього використання, що зараз досліджують.
За словами Василя Нагібіна, методи лікування, які ґрунтуються на відкритті цих клітин, ще не впроваджені в клінічну практику, хоча зараз триває близько 200 клінічних випробувань. Проте це відкриття має великий потенціал, адже може допомогти впоратися з аутоімунними хворобами й навіть боротися з деякими видами раку. Це відкриття також важливе тим, що Нобелівський комітет зазвичай присуджує премії лише за підтверджені та практично застосовані досягнення, однак у цьому випадку, попри відсутність клінічної практики, визнали потенціал відкриття. Лауреати чекали на це визнання понад 20 років, а їхні роботи, публіковані від 90-х років минулого століття, вже широко перевірені та вивчені.
За матеріалами lb.ua


